水素発生方法については、大きく分けて、2つの方法があります。電気分解方法と化学反応による方法です。どの方法も一長一短があり、今後の課題となっていくかと思います。
水素発生方法と効果的な使い方
水素発生の方法
水素発生には、大きく分けて、電気分解と化学反応の2つの方法があります。この2つの方法について説明をしていきます。
電気分解による水素発生方法
電気分解は、昔 理科の実験でも行ったと思いますが、純粋な水に電気を流しても、イオン化しないため、少しだけ、酸やアルカリに傾かせる必要があります。図は、水酸化ナトリウムで実験をしていますが、塩酸や硫酸でも大丈夫です。
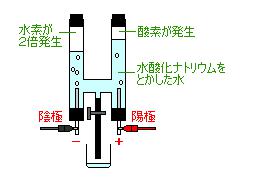
電気分解をして酸素と水素を発生させます。
2H2O ⇒ 2H2 +O2
通常陽極に酸素が、陰極側に水素が発生します。式からもわかる通り、水素発生量は、酸素の2倍発生します。また陰極側に還元水が、陽極側に酸性水が出来てくるのです。この場合、水を両方を行き来するため、混ざってしまいますが、中心部分にイオン交換膜等をいれて、水の行き来を無くしてやった場合、陰極の還元水と陽極側の酸性水を作る事ができます。
電気分解式と言われているものは、イオン交換膜で、酸性水と還元水とを分けながら電気分解したもので、還元水側の水を水素水として使っています。また電気分解で、発生させた、水素ガスを水に溶け込ます、気体過飽和式の水素水の場合は、イオン交換膜等の必要はないため、発生した、水素をバブリング等で、原水に溶けこのす事で作り出しているのが、一般的に気体過飽和方式といわれている物です。電気分解の場合は、水素飽和濃度である、約1.6ppm以上の水素濃度は得られないが、気体過飽和方式の場合は、一定容器内に気体を押し込めることで、内部気圧があがり、水素濃度の高い水素水が可能になります。
一方て゛電気分解方式で、発生する、原水中の還元力のある、ミネラルのナノコロイドは気体過飽和式では発生しません。
化学反応による水素発生方法
常温で水と反応して、水素を発生させられるものは、実は結構あります。
Na+H2O ⇒ NaOH + H2
ナトリウムと水は反応すると水素が出来ますが、一般の人ず金属ナトリウムを手に入れる事は、不可ですし、禁水物質ですので、これは爆発によっておこる反応です。
Mg+2H2O ⇒ Mg(OH)2 + H2
マグネシウムは熱水、塩水または薄い酸に溶解して、水と反応して水素を発生させる。マグネシウムは、禁水物質ですが、化学反応で水素水をつくる場合、この反応を利用しているものを見かける。二次的なものですが、水酸化マグネシウムは、緩下作用があり、便秘解消に良いものですので、水素水を飲んで、便秘解消になったのは、水素と言うよりは、同時に発生している、水酸化マグネシウムの影響が大きいような気がします。
2Al + 6H2O → 2Al(OH)3 + 3H2
アルミニウムも水と反応すると水素を出しますが、通常では、この反応はおきません、何故ならアルミニウムは、酸化皮膜が簡単に出来てしまうため、表面は酸化アルミニウムになっているからです。
そのため、このような反応で水素が発生します。
2Al+Ca(OH)2 + 6H2O ⇒ Ca(AlO4)2 +3H2
アルミに消石灰(水酸化カルシウム)と水を入れると、水素が発生します。
この反応を利用して水素水をつくっているのは、水素水7.0 や 7water などです。
そして、カルシウムも水と反応して、水酸化カルシウムと水素が発生します。
Ca+2H2O ⇒ Ca(OH)2 + H2
ただし、カルシウムもそのままで、自然界にある事はほとんど無く、水と反応して、消石灰の形になったり、さらに二酸化炭素と反応して、炭酸カルシウム、また酸素と結合して酸化カルシウムとして存在している。
また水素化物といわれる化合物が存在しており、水と反応すると、容易に水素を発生させられるものである。
固定水素化反応物質で水素発生
水素は非常に小さな元素でも有る事で、化合物の内部に入り込んでしまう事ができる物質でもある。これは化合物として存在しているのでは無く、化合物の間に入り込んでいるため、容易に取り出す事ができる状態となっており、研究が進められている。
実は天然の水素水は、水素が含まれる岩石等に地下水が通る事で、水素水を作り出していると言われています。
この水素を含む岩石は太古の地球で、酸素の無い時代で水素が高温高圧状態時に取り込まれたもので、化合物ではないため、水と接触する事で、水素が発生するのです。
これらは、化合物では無く、水素がそのベースとなった化合物に固定化されているだけだからです。水素はとても小さな元素なため、あるゆる物質の間に入り込んでしまうのです。工業製品で問題となる水素のぜい化は同様の事がおこって発生します。一方でこの性質を利用した、水素吸蔵合金などは、水素の貯蔵目的で研究がされています。
水との接触で水素発生を伴う、水素サプリメントは、フラナガン博士の考え出した、ハイドライドは、二酸化ケイ素を微粒子化したもの、九州大学白畑教授の論文より、及川博士がつくりだした、おはよう水素は、カルシウムベースの水素吸蔵品であります。両者ともに、水素のキャリアとしては、異なりますが、電気陰性度(物質の電子を引っ張りやすい性質)の強い、還元力の高いものを選択しています。ただし、水素の電気陰性度より、低い必要があります。そのバランスのおかげて、活性化した状態の原子水素または活性水素の状態を維持した状態で、水素が保持されていると言われています。
フラナガン博士は、水に溶けるレベルの微粒子化した二酸化ケイ素を水素発生のキャリアとして、その強い還元力を利用して水素の付着したパウダーを開発しました。一方で、及川博士の開発した、カルシウムベースのサプリは当初酸化還元電位も-200mVとフラナガン博士の二酸化ケイ素ベースの-600mVには、及ばなかった。しかし、ARD社は、その及川理論を昇華させて、独自製法によって、沖縄サンゴカルシウムベースの水素サプリで、酸化還元電位-600mVまで到達している。
サンゴカルシウムは、天然の多孔質体であり、比表面積が2.4m2/gと非常に大きい、また同様に牡蠣殻カルシウムも同様に、比表面積が2.05m2/gと、サンゴカルシウムに次ぐもので、酸化還元電位は-580mVまで記録されており、水素発生素材としては良質のものとなっています。
まとめ
水素発生方法は、様々な方法があり、様々な場面で活用しています。そのため、シーンに合わせた水素発生方法を選ぶ事が健康づくりに大事になります。
参考資料





“水素発生方法と効果的な7つの使い方” への11件のフィードバック